Oggi i sistemi digitali di gestione della qualità determinano l'auditabilità e la sicurezza giuridica dei processi di sterilizzazione. Chi valuta un nuovo autoclave non dovrebbe quindi limitarsi a verificare le prestazioni del processo, ma dovrebbe anche valutare sistematicamente la struttura della documentazione digitale.
Le autoclavi moderne sono spesso utilizzati per la sterilizzazione di liquidi, terreni di coltura e sostanze solide. Tuttavia, le prestazioni tecniche del dispositivo da sole non sono sufficienti. È fondamentale il modo in cui i dati del ciclo vengono registrati, memorizzati, salvati e valutati. Da ciò derivano criteri di valutazione concreti per la scelta di un sistema.
Archiviazione e integrità dei dati
Un criterio fondamentale è il luogo di archiviazione dei dati di processo. I sistemi memorizzano i dati esclusivamente nel controller del dispositivo oppure anche su un server locale o in un'infrastruttura cloud. Per i settori regolamentati è importante sapere se:
- le registrazioni elettroniche sono a prova di manomissione
- Gli audit trail vengono generati automaticamente
- I diritti degli utenti devono essere chiaramente definiti e registrati.
- le firme elettroniche sono implementate in conformità con FDA 21 CFR Parte 11
Senza queste funzioni, in caso di audit si crea un rischio. Nella scelta di un autoclave verticale è quindi necessario verificare che il controller e, se del caso, la piattaforma di gestione soddisfino pienamente i requisiti normativi.
Connettività e concetti di accesso
I sistemi digitali di gestione della qualità si differenziano notevolmente per il loro grado di interconnessione. Si possono distinguere tre modelli di base:
- Soluzione autonoma senza connessione esterna
- Rete locale con server interno
- Soluzione basata su cloud con accesso indipendente dalla posizione
Le soluzioni cloud consentono la gestione centralizzata di più dispositivi, l'accesso remoto ai dati dei cicli e la gestione degli utenti in diverse sedi. Sono adatte per organizzazioni con più laboratori o con una struttura internazionale.
Le soluzioni server locali offrono il controllo completo dei dati all'interno della propria infrastruttura IT. Sono rilevanti per le aziende con rigorose politiche interne sulla protezione dei dati o requisiti di sicurezza IT chiaramente definiti.
La decisione dipende dalla strategia IT, dai requisiti di conformità e dalla valutazione dei rischi. Un autoclave non dovrebbe quindi essere considerato isolatamente, ma come parte integrante dell'intera infrastruttura digitale.

FDA 21 CFR Parte 11 e livelli normativi
Non tutti i laboratori richiedono lo stesso grado di conformità. Nella pratica esistono requisiti graduali:
- Piena conformità alla Parte 11 per il dispositivo e il sistema di gestione
- Conformità alla Parte 11 solo a livello di dispositivo
- Documentazione senza requisiti formali della Parte 11
Questa differenziazione consente di adattare i sistemi in modo mirato alle condizioni quadro normative. Per gli ambienti di produzione GMP è richiesta la conformità totale. Negli ambienti di ricerca può essere sufficiente una conformità parziale o nessuna conformità.
Un autoclave moderno dovrebbe quindi essere concepito come una piattaforma con opzioni di gestione della qualità configurabili, non come una soluzione singola rigida.
Backup, audit trail e strategia di aggiornamento
Per una documentazione digitale affidabile è necessario verificare i seguenti punti:
- backup automatici e regolari
- Audit trail a prova di revisione
- versioni software chiaramente documentate
- Processi di aggiornamento strutturati
- Possibilità di manutenzione o diagnosi a distanza
In assenza di questi meccanismi, aumenta il carico di lavoro interno necessario per la convalida. I sistemi con funzioni integrate di backup e registrazione riducono i tempi di verifica e semplificano le riqualificazioni.
Integrazione nei sistemi esistenti
In molti laboratori sono già stati implementati LIMS, Active Directory o sistemi centralizzati di gestione degli utenti. Un'autoclave verticale dovrebbe:
- È possibile sincronizzare i ruoli utente
- Fornire formati di esportazione per LIMS
- offrire interfacce chiare per l'integrazione IT
Senza capacità di integrazione si verificano interruzioni mediali e un ulteriore onere di documentazione.
Scalabilità e gestione multi-dispositivo
Nelle strutture più grandi è importante poter gestire centralmente più autoclavi. Le piattaforme basate su cloud o server consentono di:
- Panoramica di tutti i cicli di più dispositivi
- gestione centralizzata dei programmi
- struttura utente uniforme
- valutazione trasversale alle sedi
Queste funzioni supportano processi standardizzati e riducono le discrepanze tra le sedi.
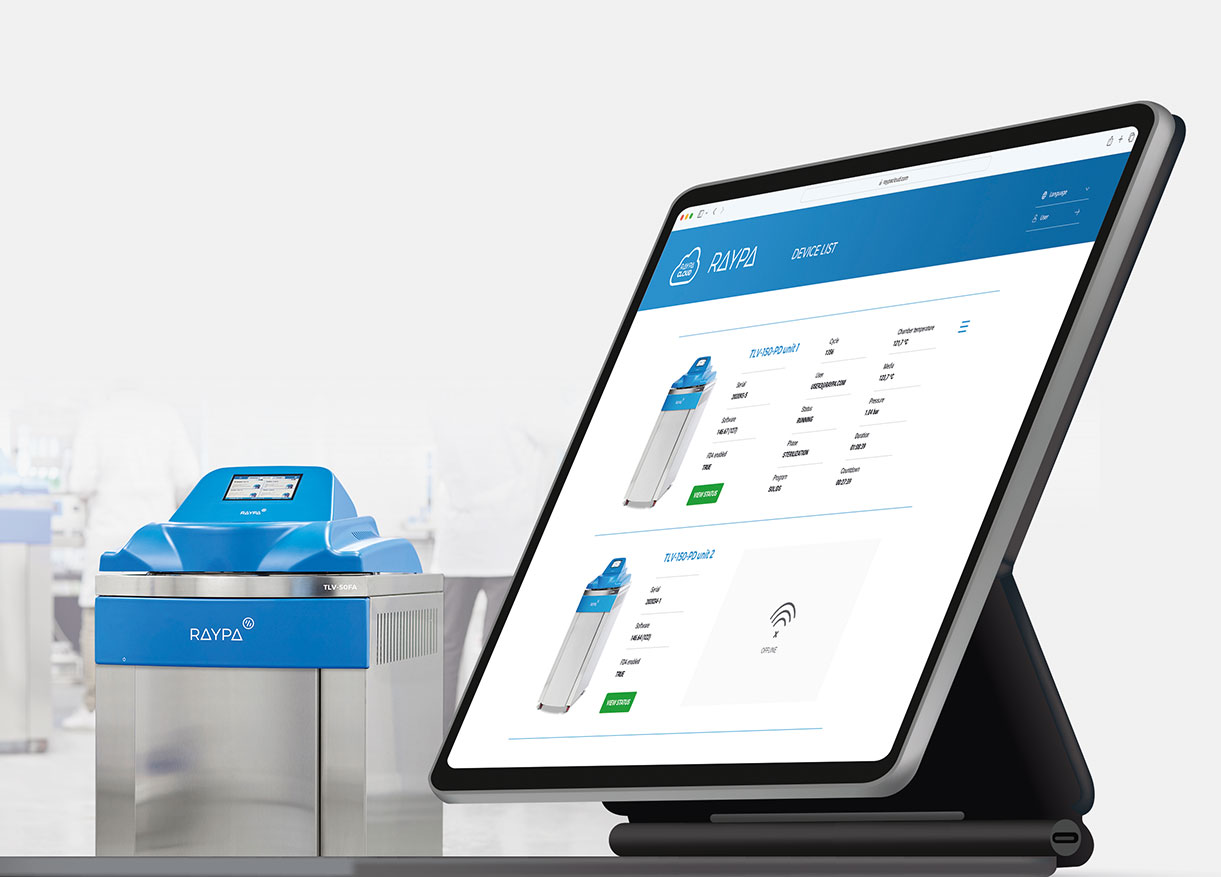
Posizionamento sul mercato
Un esempio di autoclave moderna che offre diverse opzioni di gestione digitale della qualità è la serie Raypa TLV. Il sistema offre diversi modelli di configurazione, che vanno da una soluzione puramente locale e non collegata in rete a varianti basate su cloud con funzioni di gestione avanzate.
Ciò che conta non è tanto la denominazione del prodotto quanto l'approccio strutturale. Un dispositivo di questa classe è concepito come una piattaforma modulare in cui la connettività, il livello di conformità e l'archiviazione dei dati possono essere adattati ai requisiti normativi.
Conclusioni per la scelta delle autoclavi verticali
Al momento dell'acquisto del nuovo autoclave, oltre alla pressione, alla stabilità della temperatura e al controllo del processo, è necessario valutare sistematicamente i seguenti aspetti:
- Dove vengono memorizzati i dati relativi al ciclo
- È richiesta la conformità alla Parte 11?
- Quali funzioni di audit e backup sono integrate?
- Come avviene l'integrazione nei sistemi IT esistenti?
- È necessaria una gestione trasversale alle sedi?
Le funzioni digitali di gestione della qualità non sono un modulo aggiuntivo. Esse definiscono la sicurezza operativa a lungo termine, la verificabilità e la scalabilità di un laboratorio. Chi tiene conto di questi criteri sin dalle prime fasi riduce gli oneri di convalida e aumenta la trasparenza dei processi di sterilizzazione.
Panoramica del prodotto

Serie TLV-DUAL
- Con sistema di superessiccazione e raffreddamento rapido
- Autoclave verticale
- Massima flessibilità (liquidi e solidi)
- Volumi lordi: 58, 83, 124, 169 L
- Opzionale con filtro HEPA per rifiuti biologici pericolosi
- Con generatore di vapore

Serie TLV-FA
- Con sistema di raffreddamento rapido
- Autoclave verticale
- Ideale per la sterilizzazione di liquidi
- Volumi lordi: 58, 83, 124, 169 L
- Opzionale con filtro HEPA per rifiuti biologici pericolosi
- Con generatore di vapore

Serie TLV-PD
- Con sistema di superessiccazione
- Autoclave verticale
- Ideale per la sterilizzazione di vetro, solidi porosi e oggetti con
- Volumi lordi: 58, 83, 124, 169 L
- Opzionale con filtro HEPA per rifiuti biologici pericolosi
- Con generatore di vapore

Serie TLV-S
- versione base
- Autoclave verticale
- Volumi lordi: 58, 83, 124, 169 L
- Opzionale con filtro HEPA per rifiuti biologici pericolosi
- Con generatore di vapore
Trova l'autoclave più adatta al tuo laboratorio
Utilizzate lo strumento di selezione di RAYPA. Filtrate le autoclavi in base alla tecnologia, all'applicazione e ai requisiti di tracciabilità. La funzione di filtro avanzata vi guida in pochi passaggi verso l'apparecchio più adatto. Scegliete in modo mirato i modelli che si adattano ai vostri processi, al vostro volume di campioni e ai requisiti normativi del vostro laboratorio.
Vuoi saperne di più sulla serie RAYPA TLV?
Saremo lieti di fissare immediatamente un appuntamento con voi.



